近日,复旦大学附属华山医院神经外科周良辅院士团队在国际知名期刊《Journal for ImmunoTherapy of Cancer》(IF=10.6)上发表了一项脑胶质瘤免疫治疗创新研究成果,提出了经脑室内注射(ICV)神经干细胞(NSCs)搭载溶瘤病毒(OV)治疗胶质母细胞瘤(GBM)的新策略(NSCs-OV)。该策略显著提升了溶瘤病毒对肿瘤的靶向性和治疗安全性,拓展了调控肿瘤免疫微环境增强抗肿瘤效应的新路径。

胶质母细胞瘤(GBM)是中枢神经系统最常见、最具侵袭性的恶性肿瘤,患者中位生存期仅12-15个月,临床治疗手段极为有限。尽管溶瘤病毒(OV)疗法在肿瘤选择性杀伤和免疫激活方面展现出潜力,但临床应用面临病毒递送效率低、免疫清除快、肿瘤浸润性差三大瓶颈。周良辅院士团队创新性利用神经干细胞作为“特洛伊木马”,结合脑室给药途径,成功实现了溶瘤病毒在中枢神经系统的高效、精准投递。
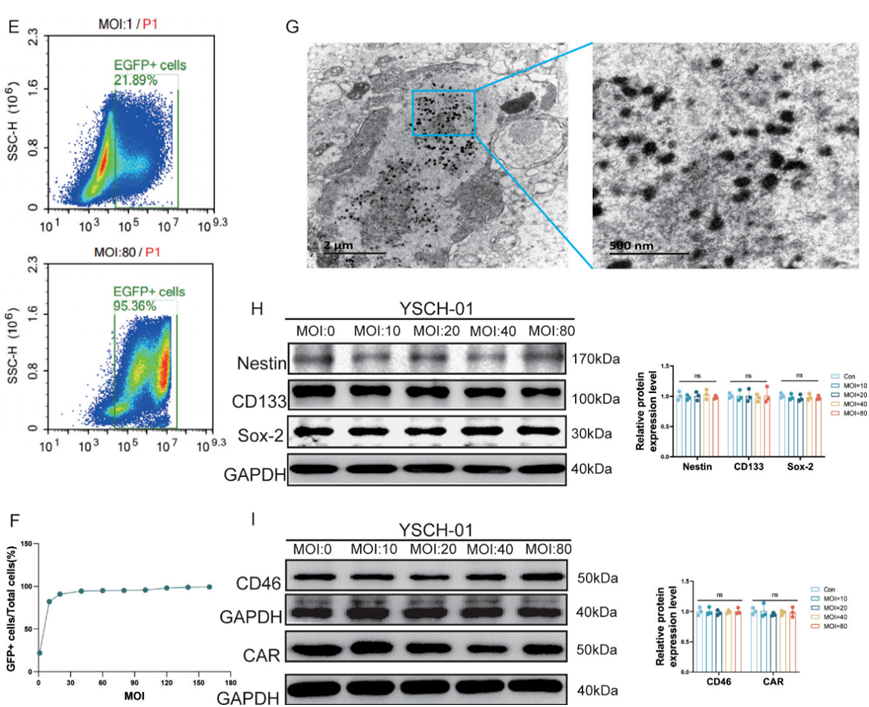
研究团队证实了神经干细胞在感染溶瘤病毒后仍能保持其干性特征和迁移能力,且病毒复制未影响其干细胞特性。体外实验中,NSCs-OV显著抑制了胶质瘤细胞的迁移、增殖与克隆形成能力,展现出比单一病毒治疗更强的抗肿瘤效果。更重要的是,研究团队建立了一套体外脑室给药模拟系统,证实NSCs-OV在血清环境中仍能保持病毒稳定性,有效避免中和抗体的清除作用。
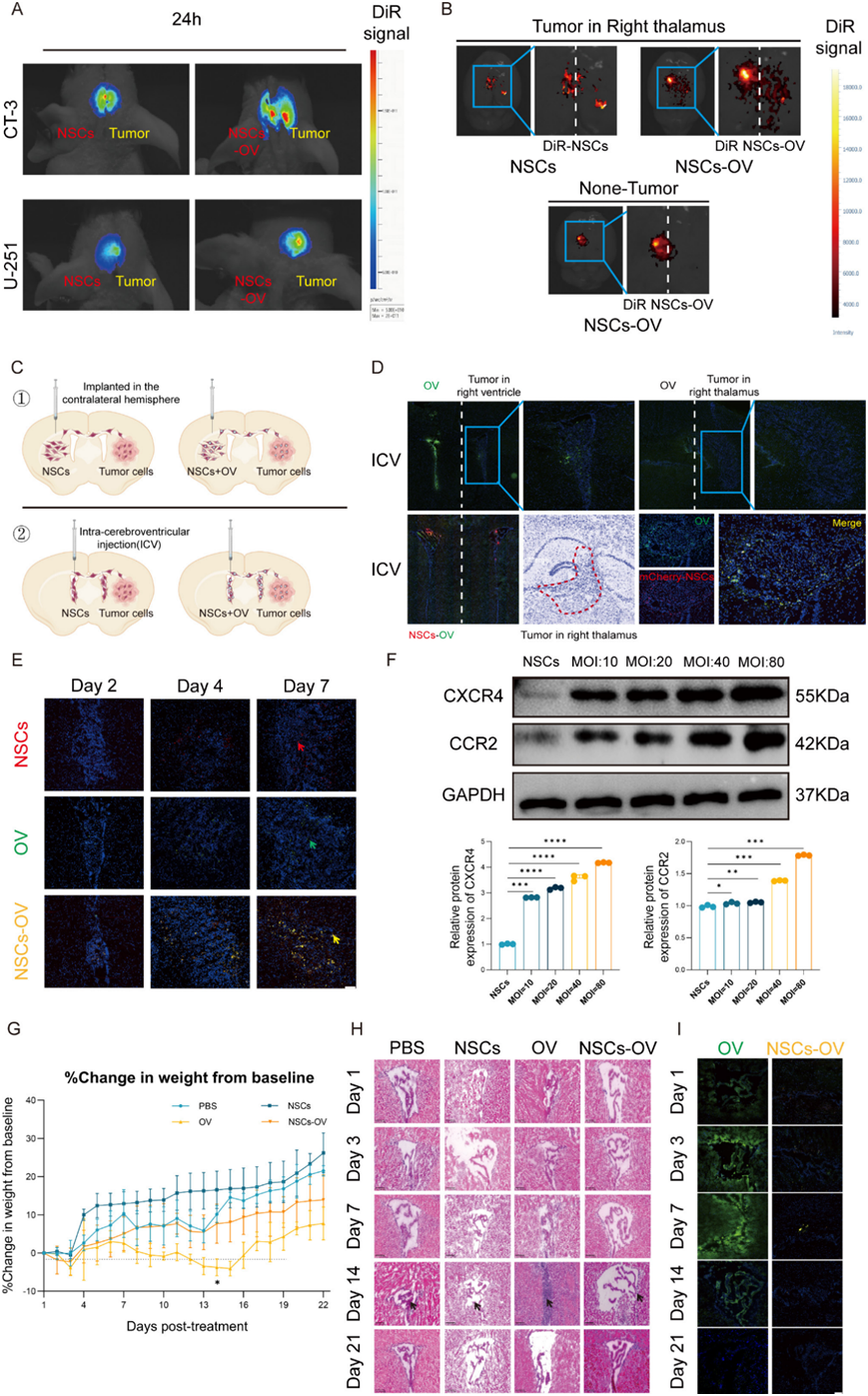
在动物实验层面,通过构建原位胶质瘤模型,发现经ICV注射的NSCs-OV能够快速迁移至肿瘤部位,在24小时内实现广泛分布。与直接注射病毒相比,NSCs-OV组表现出更强的肿瘤靶向性和更持久的病毒滞留效应,有效延长了治疗作用时间。
安全性评估显示,NSCs-OV治疗显著降低了单纯病毒治疗引起的炎症反应和系统毒性。组织病理学分析表明,NSCs保护了脑室壁结构完整性,避免了病毒直接暴露引起的室管膜损伤和水肿形成,体现了良好的安全性特征。
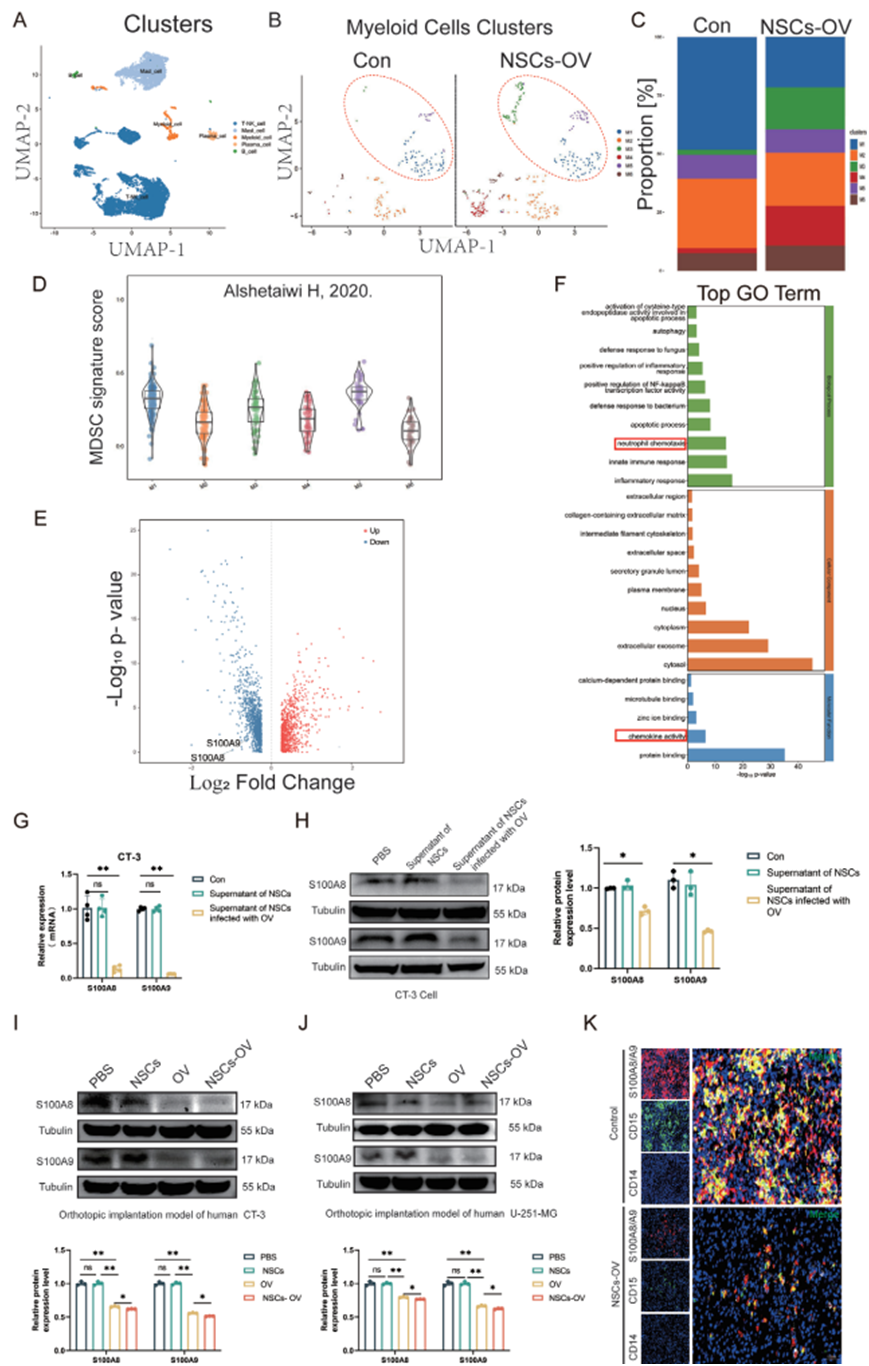
机制研究发现,NSCs-OV治疗能够显著下调肿瘤微环境中S100A8/A9的表达,这两个分子是髓系来源抑制细胞(MDSCs)的关键趋化因子和免疫抑制介质。单细胞测序分析显示,NSCs-OV治疗后MDSCs比例显著降低,同时CD8+T细胞浸润增加,表明肿瘤免疫微环境从免疫抑制状态向免疫激活状态转变。
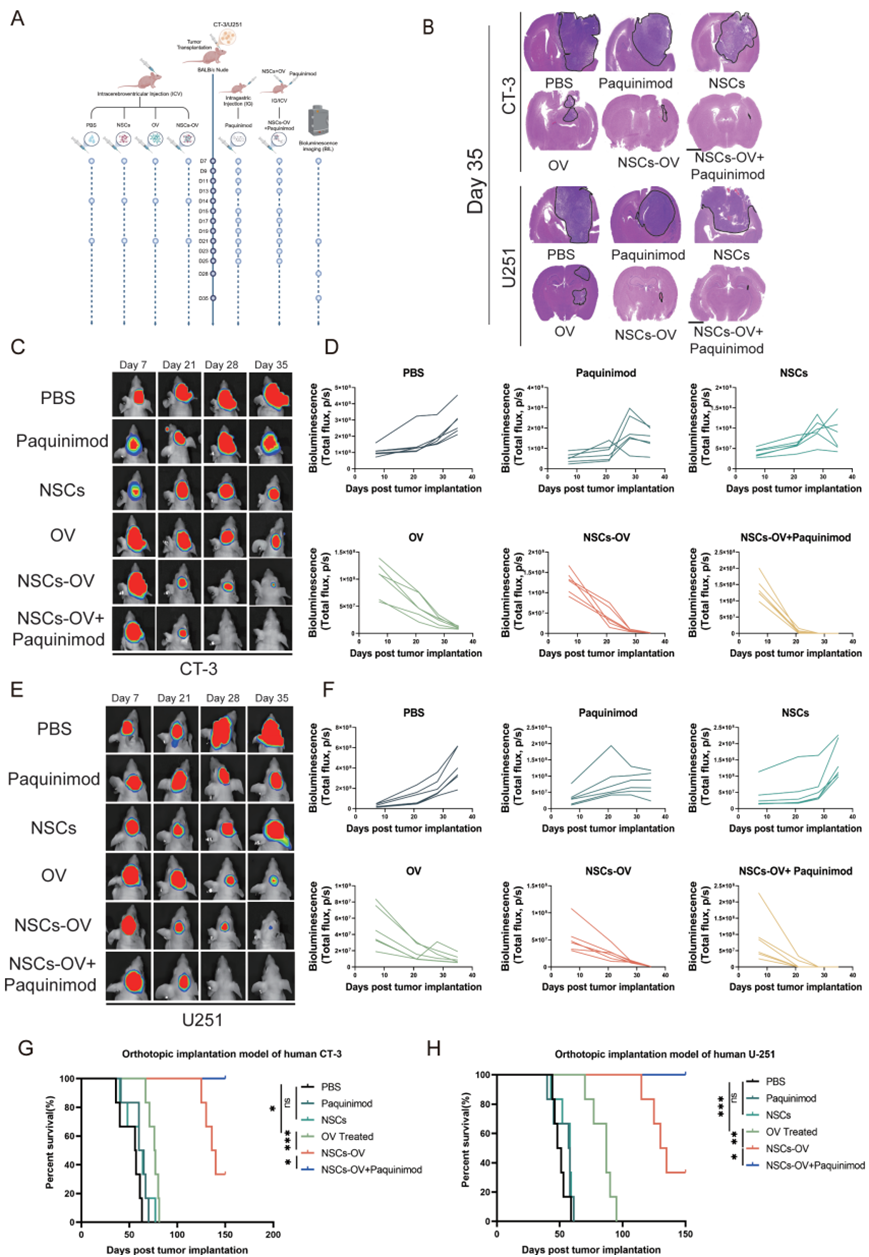
此外,研究还发现NSCs-OV与S100A8/A9抑制剂帕喹尼莫德联用可产生协同增效作用,进一步抑制肿瘤生长并延长生存期。这种联合策略为临床开发新型组合治疗方案提供了重要理论依据。
这项研究的创新点在于首次将神经干细胞载体技术与脑室内给药途径相结合,不仅解决了溶瘤病毒在中枢神经系统递送效率低的问题,还通过调控肿瘤免疫微环境,实现了从单纯病毒治疗到免疫协同治疗的跨越。
该研究成果不仅为胶质母细胞瘤患者提供了新的治疗希望,也为其他中枢神经系统肿瘤的治疗开辟了新思路。研究团队目前正在进一步优化该技术方案,推动其向临床应用转化,期待早日惠及广大患者。
复旦大学附属华山医院神经外科柴辉辉博士为本文的第一作者,周良辅院士、史之峰教授为本文的通讯作者。
论文信息:Chai H, Xu H, Jiang S, et al. Neural stem cell-delivered oncolytic virus via intracerebroventricular administration enhances glioblastoma therapy and immune modulation. Journal for ImmunoTherapy of Cancer 2025;13:e012934. doi:10.1136/jitc-2025-012934
原文链接:https://jitc.bmj.com/content/13/10/e012934
