近日,复旦大学附属华山医院神经外科周良辅院士、史之峰教授团队在国际神经肿瘤学顶级期刊《Neuro-Oncology》(中科院1区Top,IF=16.4)发表重要研究成果。该研究依托创新性的RESCUE临床转化研究框架,首次揭示了复发胶质瘤在溶瘤病毒免疫疗法压力下构筑“肿瘤隔离带(Tumor Self-Rampart)”这一空间治疗抵抗机制,并提出了能够指导临床精准用药的协同用药方案,为打破脑肿瘤免疫治疗僵局开辟了新路径。

Shan Jiang, Houshi Xu, Maoyuan Sun, Yongfen Xu, Huihui Chai, Zhen Fan, Zhirui Zhou, Beining Liu, Yue Wang, Ruize Zhu, Jiawen Chen, Yun Guan, Xin Wang, Yulai Zeng, Zhen Li, Weiqiu Ping, Yanlin Teng, Songlin Yan, Tianwen Li, Qisheng Tang, Kangjian Zhang, Zanyi Wu, Bojie Yang, Yifang Ping, Liangfu Zhou, Zhifeng Shi, IL-8-Induced Tumor Self-Rampart Spatially Confines Oncolytic Virotherapy in Glioblastoma, Neuro-Oncology, 2025; noaf276
https://doi.org/10.1093/neuonc/noaf276
临床痛点:溶瘤病毒的“后继乏力”
近年来,溶瘤病毒疗法(OV)作为一种通过特异性感染并裂解肿瘤细胞的新型免疫疗法,在胶质母细胞瘤(GBM)的治疗中展现出了巨大的应用潜力。但在临床实践中发现,病毒在进入颅内肿瘤后往往面临着“后继乏力”的窘境,导致长期疗效难以维持。由于人脑结构的封闭性,临床试验无法像外周实体瘤那样频繁地进行组织活检,这使得颅内病毒复制的实时状态成为了一个难以观测的“黑箱”,严重限制了对患者疗效敏感标志物的预测以及长期生存获益机制的探索。
策略创新:RESCUE框架下的“逆转化”研究
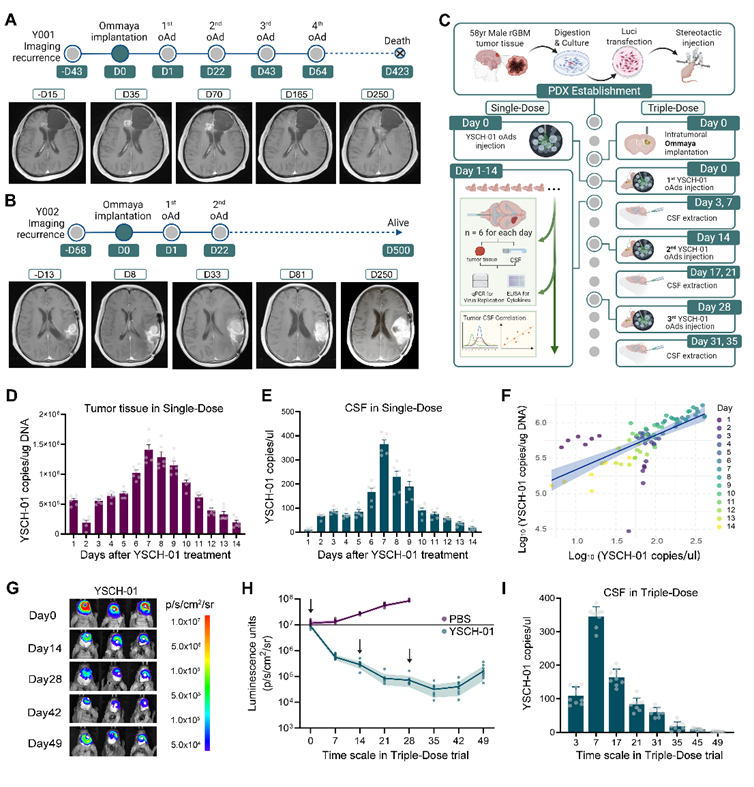
为了破解这一阻碍溶瘤病毒新疗法临床转化的核心瓶颈,华山医院周良辅院士与史之峰教授团队建立了一套“RESCUE(Reverse Engineering & Scrutinizing of Clinical Urgent Events)”转化研究框架。研究团队以新型溶瘤腺病毒YSCH-01临床试验为基准,同步构建了患者来源的异种移植(PDX)模型。利用PDX动物模型在实验室中“复刻”临床患者的治疗过程,通过肿瘤替身弥补临床试验中样本数量有限的局限。
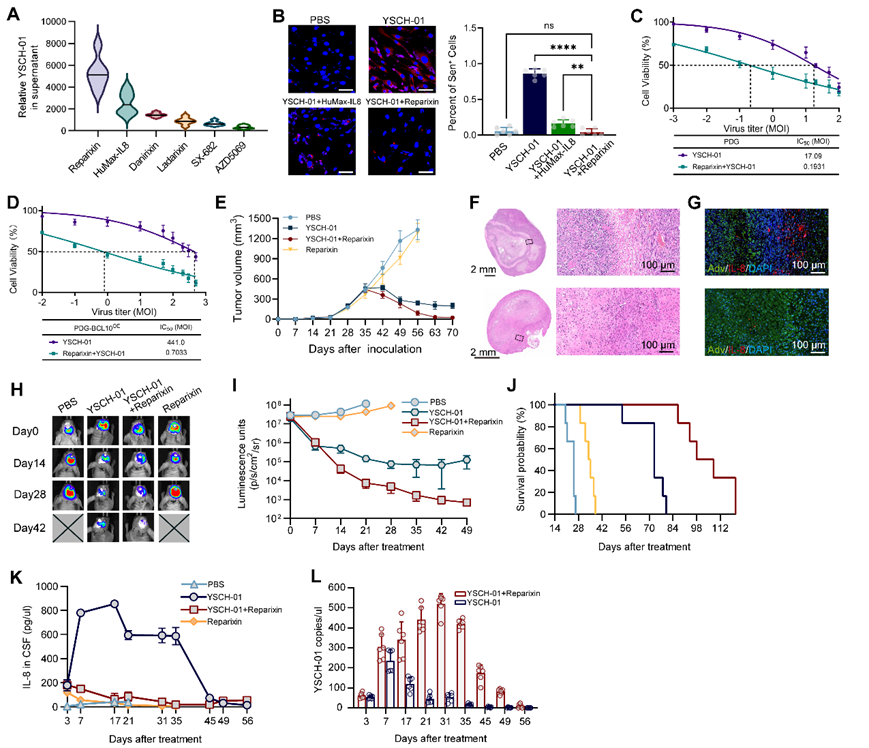
在RESCUE策略的指引下,研究团队首先利用颅内置管的PDX小鼠模型,刻画颅内胶质瘤瘤内病毒复制动力学。溶瘤腺病毒在单次瘤内给药后,会经历第3天和第7天两次复制高峰,随后病毒滴度快速下降。在多次给药模式中,每次给药后的第二次复制效能均呈现出显著下跌,且并非中和抗体所致。为了深入探究造成这一“复制受限”背后的分子机理,团队开展了全基因组CRISPR激活文库筛选发现,当溶瘤病毒感染肿瘤细胞后,会激活BCL10基因,进而通过NF-κB信号通路诱导细胞因子IL-8的旁分泌,进而诱导临近未感染病毒的肿瘤细胞提前进入衰老状态。
机制解析:肿瘤的“焦土策略”与“空间隔离”
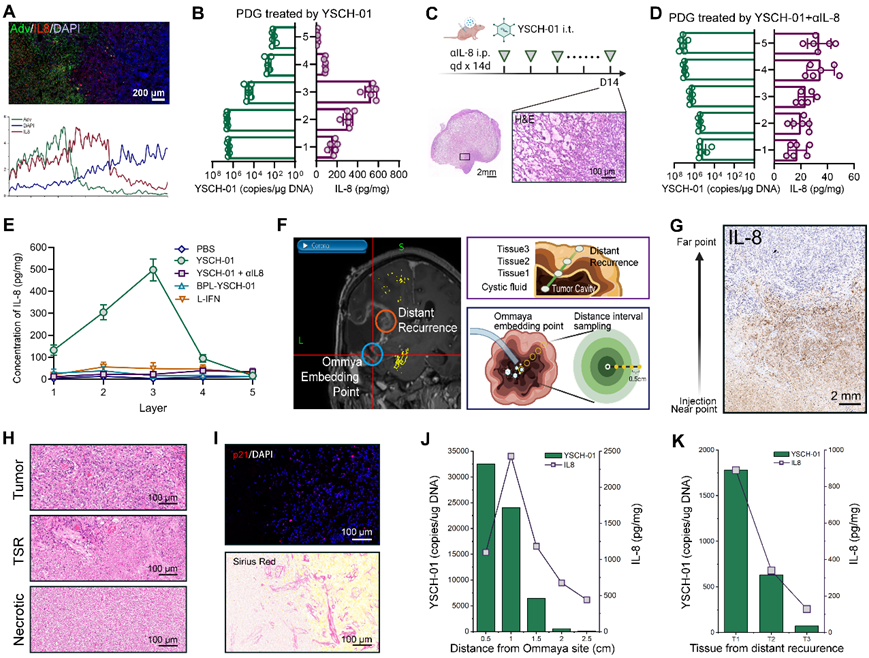
空间转录组学进一步解析了这一过程:由IL-8诱导的衰老肿瘤细胞,在溶瘤病毒治疗造成的坏死区域周边迅速聚集重塑构筑一层“肿瘤隔离带”结构,呈现出高度纤维化的特征,构成了病毒扩散的物理屏障。与此同时,衰老肿瘤细胞的病毒复制能力显著下降形成生物屏障,极大地阻断了其在胶质瘤组织中的扩散距离,进而限制了病毒的复制滴度和复制轮数。这种肿瘤自我重塑的“肿瘤隔离带”在接受溶瘤病毒临床试验治疗的患者肿瘤组织中也被观测到。
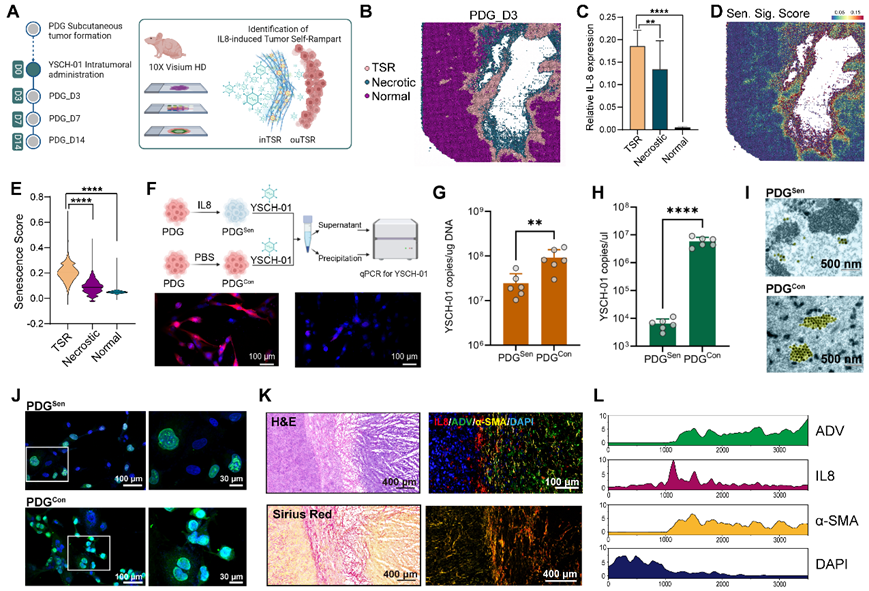
临床转化:打破隔离,精准增敏
基于对“肿瘤隔离带”机制的时空解析,研究团队通过药物筛选得到IL-8受体的靶向抑制剂——Raperixin。与溶瘤病毒的联合使用,有效抑制了隔离带的形成,显著增敏了溶瘤病毒的复制效力。这一发现为开发针对胶质瘤的新型联合免疫疗法提供了确凿的药物靶点。此外,通过RESCUE策略的模拟,研究团队发现,在给药早期使用糖皮质激素不仅不会由于免疫抑制而影响病毒疗效,反而因为其抗炎作用,有利于消除由炎症因子IL-8驱动的“隔离带”形成,从而辅助病毒更好地扩散。这一发现回答了胶质瘤免疫临床试验中关于病房精准用药的迫切需求。