近日,复旦大学附属华山医院神经外科朱巍教授团队携手复旦大学生物医学工程与技术创新学院、华山医院放射科,于脑血管病领域著名期刊Stroke and Vascular Neurology(IF=4.9,JCR Q1)在线发表题为“Multimodal MRI habitat atlas for personalised re-haemorrhage risk prediction in brainstem cavernous malformations”的研究文章。复旦大学附属华山医院神经外科朱巍教授、全凯医师,复旦大学生物医学工程与技术创新学院马煜副教授为本文共同通讯作者。

doi:10.1136/svn-2025-004701
PMID: 41638756
脑干海绵状血管畸形(Brainstem Cavernous Malformations,BSCM)具有高出血风险和高致残率,既往前瞻性研究提示中患者首次出血后2年内的年再出血风险高达26.3%-42.4%。然而,显微手术或放射外科治疗存在5%-35%的治疗后神经功能缺损风险。因此,对于BSCM患者,选择合适治疗方案的核心就在于,精准识别高出血风险病灶,根据未来出血风险大小制定个体化诊疗策略。
在BSCMs未来出血风险的预测因子中,已发现的最强预测因子是既往的症状性出血史以及特定的定性MRI表型,例如Zabramski I型分类。然而,传统影像组学模型在预测BSCMs再出血时面临着巨大挑战:传统的医学影像组学依赖对病灶整体宏观纹理特征的识别提取,但在BSCM中,血红蛋白降解产物状态会随时间发生动态演进(血肿吸收、含铁血黄素沉积等),掩盖病理状态下真实的血管解剖结构,并导致影像组学特征随时间变得不稳定,干扰传统的影像分析;此外,出血后海绵状血管畸形病灶本身容易与周围血肿边界混淆,在小样本量下模型极易发生过拟合问题。
针对上述问题,本研究借鉴肿瘤影像学中的“生境(Habitat)”分析理念,将其应用于BSCM的MRI评估。该方法的核心思路是:利用多参数MRI的无监督聚类,将病灶内部划分为若干具有生物学可解释性的亚区,每个亚区内部的多参数MRI信号特征趋于一致,而不同亚区之间则体现出病灶内部的组织异质性。由于这种基于体素信号分布的空间划分方式反映的是病灶的内在组织学构成,而非某一时间点血红蛋白降解产物的信号强度,因此理论上可在不同出血阶段保持相对稳定的特征表达。基于上述所言,本研究旨在:(1)构建一套跨出血阶段稳定的BSCM MRI生境图谱,以标准化病灶内部结构的定量描述;(2)整合生境衍生的影像学标志物与临床变量,建立并验证一个用于个体化再出血风险评估的多模态预测模型。
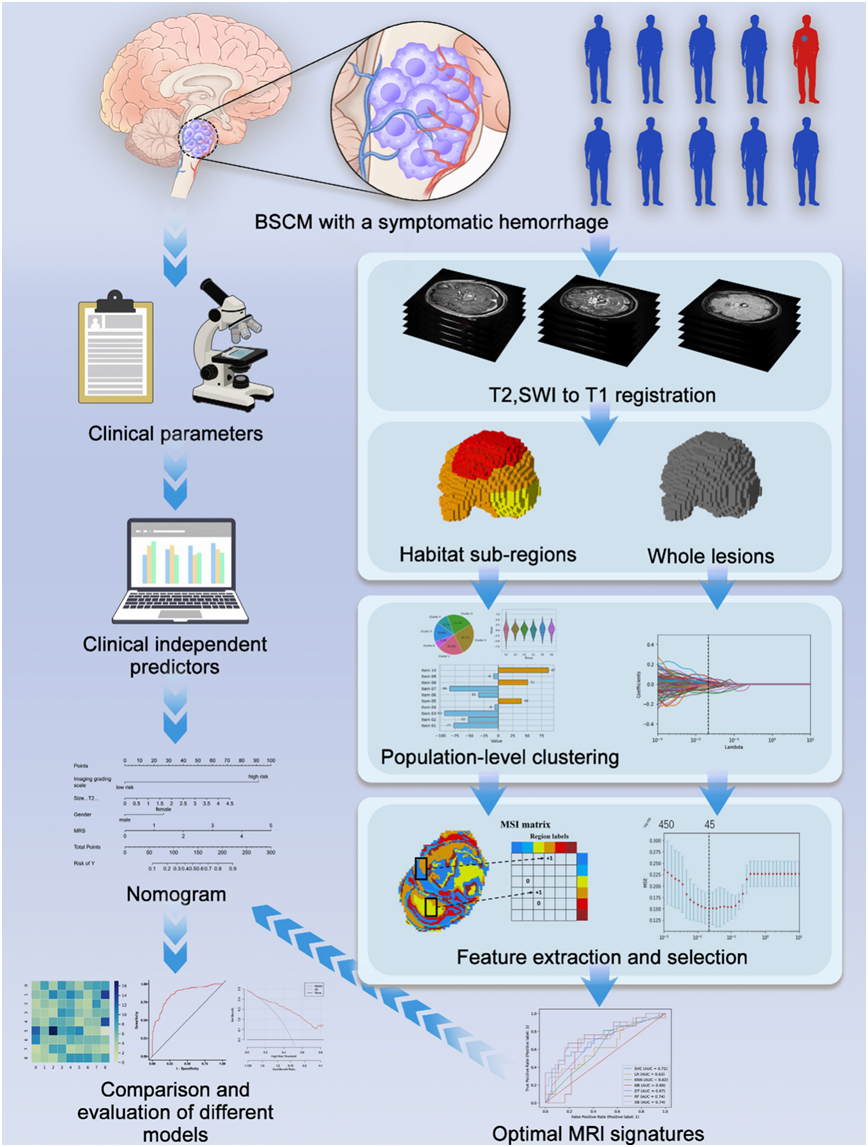
图1:临床-影像多模态BSCM再出血预测模型开发流程。
本研究纳入两个独立队列共299例BSCM患者。回顾性队列来源于华山医院总院(2015年1月至2020年12月),共205例符合纳选标准的患者,按7∶3的比例随机分配至训练集(n=147)和内部验证集(n=58)。前瞻性时间验证队列来源于华山医院西院(2021年1月至2023年6月),共94例,作为独立的外部测试集。纳入标准包括:经MRI证实的BSCM(具有典型“爆米花”样外观及T2低信号含铁血黄素环)、基线MRI后至少12个月的无干预观察期(或在此期间内发生再出血)、年龄≥18岁。排除标准包括:就诊时即因症状性出血需行急诊手术者、放射诱导型海绵状血管畸形、凝血功能障碍或正在接受抗凝/抗血小板治疗(低剂量阿司匹林除外)以及Zabramski IV型病变。两组队列在性别构成、BMI、病灶多发性及Zabramski分型等基线特征上差异无统计学意义,提示队列间具有较好的同质性。
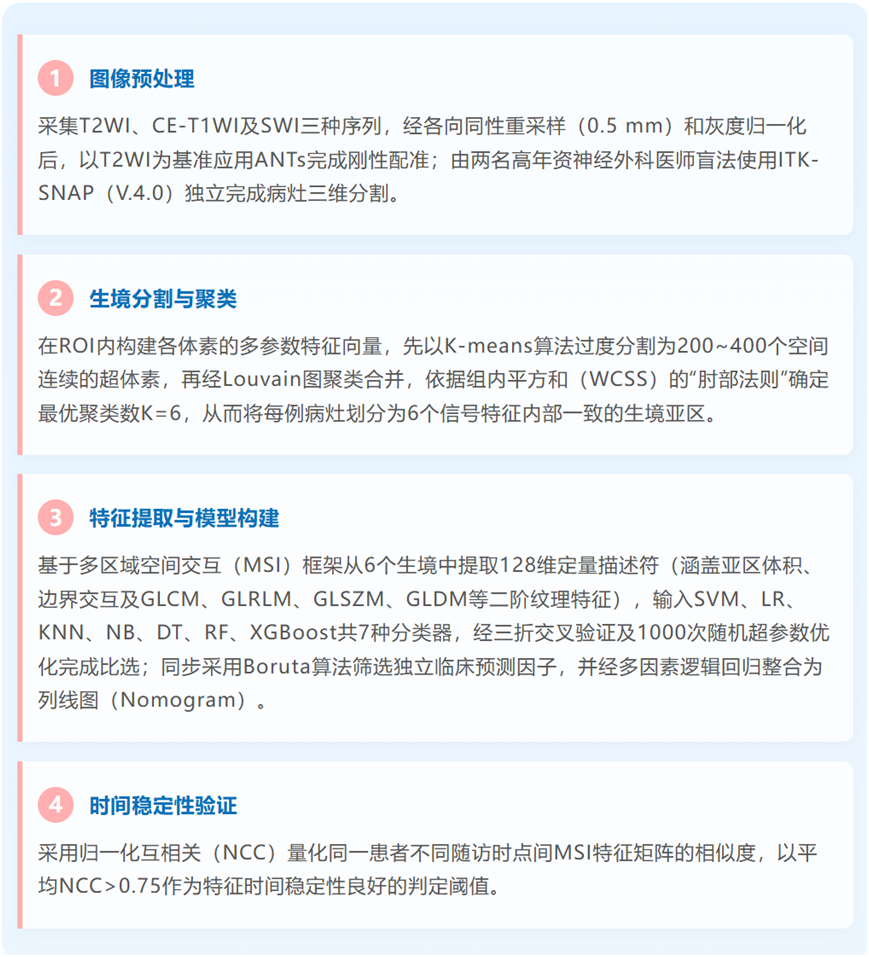
本研究的分析与建模流程主要包含以下四个步骤:

1.生境图谱的时空稳定性与生物学特征。UMAP降维分析显示,6个生境亚区在特征空间中呈非重叠分布并具有可辨识的影像学特征:如聚类1以T2_ZonePercentage升高、T1_Maximum及T1_90Percentile抑制为主,提示慢性含铁血黄素沉积;聚类6则以T1_90Percentile和T1_DependenceEntropy升高为特征,符合急性/亚急性出血表现。纵向随访病例中,MSI特征矩阵的平均NCC>0.75,证实生境衍生特征在血红蛋白降解产物动态演变背景下仍具有良好的时间稳定性。基于影像风险评分的分层结果显示,高风险组2年累积再出血率为81%(101/125),低风险组为26%(45/174),差异具有统计学意义(Log-rank P<0.001)。
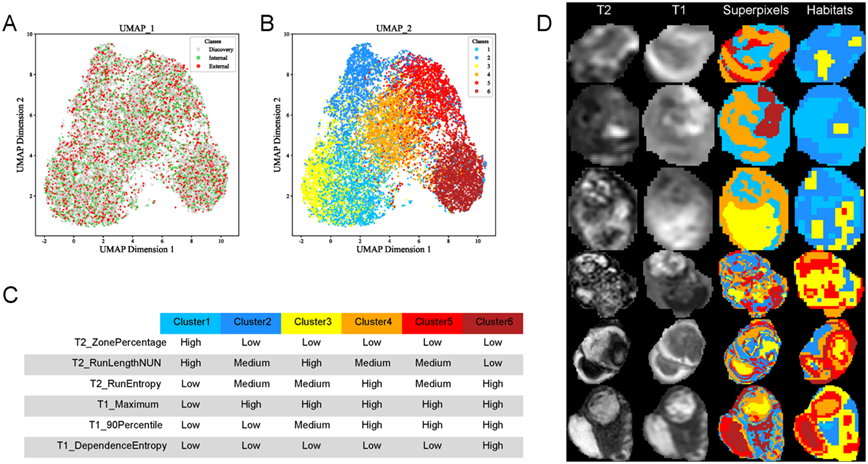
图2:基于MRI的BSCM生境聚类。
2.机器学习模型选择。7种候选模型中XGBoost判别效能最佳,训练集、内部验证集及外部测试集AUC分别为0.81(95%CI: 0.780.85)、0.80和0.82(95%CI: 0.750.89),且显著优于传统全病灶影像组学模型(AUC 0.82 vs. 0.73)。SHAP归因分析显示MSI116_gldm_DependenceNonUniformity和MSI69_glcm_ldmn为权重最高的预测特征,其重要性排序在外部验证集中高度一致。广义相加模型(Generalized Additive Model, GAM)进一步证实影像风险评分与再出血log-odds呈严格线性关系(edf≈1.0,P<0.001),未见阈值或饱和效应,支持其作为连续型预测变量的可靠性。
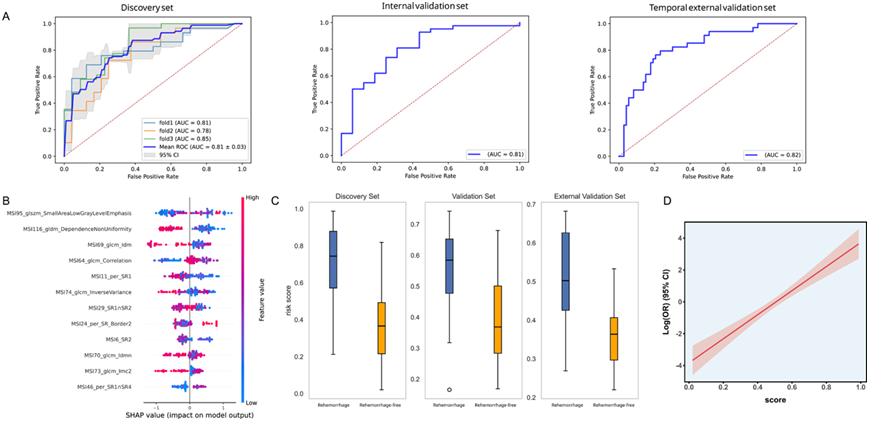
图3:基于多区域空间交互(MSI)特征的XGBoost模型在再出血预测中的效能及可解释性。
3.多模态列线图的构建与验证。Boruta算法筛选出女性(OR=2.82,95%CI: 1.425.80)、BMI(OR=1.10,95%CI: 0.991.25)及入院mRS评分(OR=2.11,95%CI: 1.343.41)为独立临床预测因子。整合上述变量与影像风险等级后,多模态列线图在训练集和外部验证集的AUC分别达0.833(95%CI: 0.7770.889)和0.851,显著优于单纯影像模型(ΔAUC=+0.07,P=0.008)和单纯临床模型(ΔAUC=+0.17,P<0.001);自举法校正C-index为0.816,Hosmer-Lemeshow检验示校准度良好(P=0.29),决策曲线分析提示在5%~75%阈值范围内临床净获益最大。亚组分析进一步显示,女性(校正OR=2.89,P=0.008)、较大病灶体积(校正OR=1.87,P=0.025)及较高mRS评分(校正OR=1.84,P=0.005)仅在低风险亚组(n=174)中与再出血显著相关,而在高风险亚组(n=125)中上述临床变量均无统计学关联(均P>0.05),提示影像学高风险病灶的再出血可能更多取决于病灶自身的内在生物学特性而非传统临床指标。
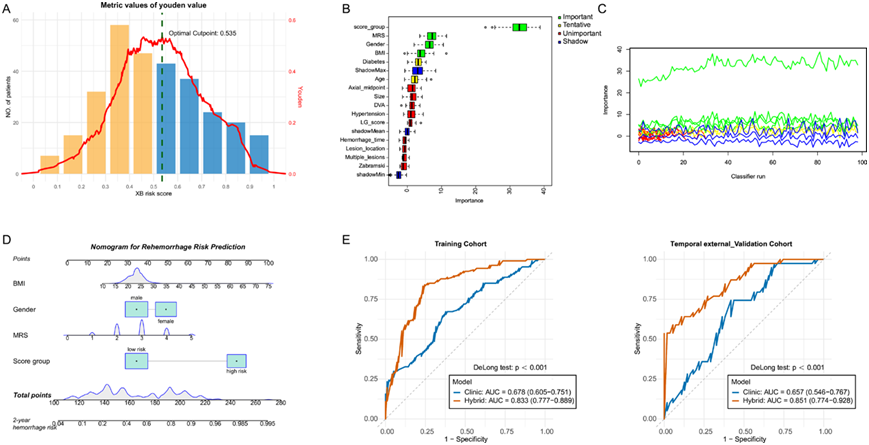
图4:BSCM再出血风险预测的多模态临床-影像列线图的开发、解读与验证。
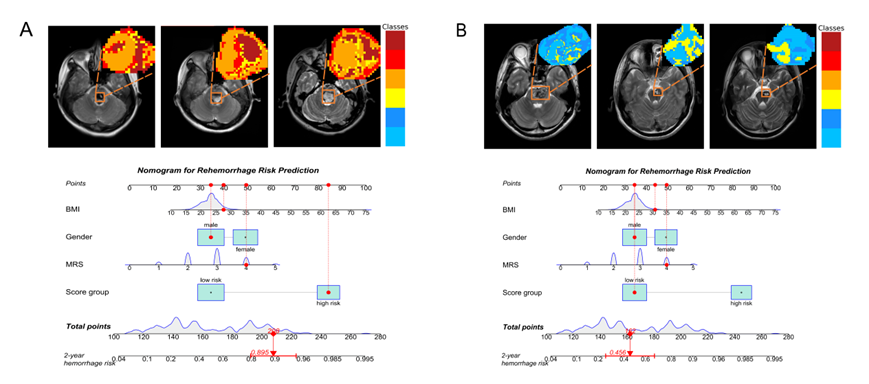
图5:典型病例展示。病例A:59岁男性,初诊mRS 4分,分别于随访第3个月和第5个月发生症状性再出血。三个时间点的生境分析均显示聚类4-6占据主导地位(平均NCC=0.85),列线图预测其2年再出血概率为0.895。病例B:48岁男性,初诊mRS同为4分,但随访1年和2年时病灶体积缩小、出血吸收,未发生再出血。其生境图谱以聚类1-3为主(平均NCC=0.82),列线图预测2年再出血概率为0.456。两例患者入院时临床状态相似,但生境图谱揭示了病灶内部微结构组成的本质差异,据此给出了截然不同的风险预判。

